何为罕见病?
罕见病是指流行率很低、很少见的疾病,一般多为慢性、严重性疾病,常危及生命。《中国罕见病定义研究报告2021》报告中首次提出了将“新生儿发病率小于1/万、患病率小于1/万、患病人数小于14万的疾病”列入罕见病。
罕见病的发病率虽然很低,但种类较多,全球约有7000种罕见病,影响着世界约7%的人口。80%罕见病是由遗传因素引起(如原发性高草酸尿症、苯酮尿症、白化病、线粒体病、血友病等),其中儿童发病的比例过半。
由于其患者基数少,大多数医生相关临床经验较少,罕见病的患者可能会有被漏诊或误诊的情况。更值得关注的是:罕见病机制研究相对滞后,其药物开发往往会相对缓慢,而且相关药物开发后市场相对较小。罕见病药物有一个令人闻之心酸的别名—“孤儿药”。目前90%以上的罕见病没有有效的治疗方法。长期以来罕见病患者面临着可用药品相对不足,药价较高、负担较大,病情危重难以诊治的困境。
近几年,我国医保重点关注了罕见病用药,纳入目录的罕见病药品数量有所增加、覆盖的罕见病病种也在扩大,如:包括用于多发性硬化的氨吡啶缓释片、用于法布雷病的阿加糖酶α注射溶液、治疗脊髓型肌萎缩症的诺西那生钠注射液、治疗血友病的人凝血因子IX等。
小核酸药物:”ASO”or”siRNA”
当前罕见病药物的形式包括小分子药物、抗体药物、小核酸药物等。小核酸药物由序列经过特定设计的核苷酸组成,由于近些年核酸的修饰和递送载体技术的突破,使得小核酸药物成为现在治疗罕见病的有效手段。
临床使用或开发中的小核酸药物主要包括反义寡核苷酸(antisense oligonucleotides,ASO)或siRNA(small interfering RNA)。ASOs和siRNA都通过碱基互补配对结合靶基因的mRNA或pre-mRNA,但其组成和作用方式不同。
■siRNA
是一种小的外源性双链RNA(dsRNA),约有20-25个核苷酸长度,siRNA进入细胞触发了RNA干扰机制:dsRNA解旋后正义链被降解,反义链与多种蛋白组分形成RNA诱导的沉默复合体(具有核酸酶活性)(RNA Induced Silencing Complex,RISC)。RISC中保留的反义链与靶基因的mRNA特异地互补,将靶基因的mRNA切割降解,从而抑制靶基因的表达,导致目标基因功能丧失(图1b)。
图 1.核酸类药物的作用机制
a.DNA到RNA 的转录机制b. siRNA 的作用机制 c.ASO 的作用机制
■反义寡核苷酸(ASO)
通常指通过化学合成生产的短单链DNA或RNA(8-50个核苷酸长度)。反义寡核苷酸(ASO)与成熟mRNA结合阻止其附着在核糖体上,阻断蛋白质翻译或招募RNaseH引起mRNA的降解(图1c,作用方式1)。ASO与pre-mRNA结合改变剪接因子的招募,从而调节剪接事件(图1c,作用方式2)。
■小核酸药物的特点
理论上,小核酸药物能够靶向任何基因,这为小核酸药物的研发提供了丰富的候选靶点,包括很多传统药物无法成药的靶点(比如说那个药物或者靶点)。此外,小核酸药物的设计摆脱了传统药物的大规模筛选,大大地缩短了药物开发的周期。
尽管小核酸药物具有很好的治疗,但也面临一些挑战:由于核酸的分子量较大,小核酸药物不能自己进入细胞。此外,裸的核酸在血液中容易被核酸酶降解,还可能激活TLR3/7/8,RIG-I和MDA-5等模式识别受体。这些因素都可能限制小核酸药物的的治疗潜力。
■针对小核酸药物的“策略”
载体包裹:将小核酸药物包裹在脂质纳米颗粒(Lipid Nanoparticle,LNPs)中,以解决药物递送问题。
这些脂质纳米颗粒中通过胞吞作用进入细胞,纳米颗粒通常用胆固醇或聚乙二醇(PEG)等基团修饰,有助于掩盖核酸携带的电荷,保护其不被核酸酶降解(图2)。还有一些纳米颗粒通过添加靶向部分(通常是靶向细胞表面受体的配体)来定向到特定的细胞。
图2.LNP制剂在系统用药后的作用机理[5]
2’化学修饰:这种方法同样可以帮助小核酸药物高效的递送,2’化学修饰 (2′-F、2′-OMe和2′-MOE等) 的掺入降低核酸酶降解小核酸药物的能力,同时也显著降低了TLR-3/7/8识别小核酸药物为外源性核酸的能力。
2’化学修饰大大提高了核酸的稳定性和整体半衰期,实现了裸的小核酸药物与靶向结构域直接偶联,从而避免了脂质纳米颗粒的使用。此外,一些小核酸药物还会在3’末端偶联GalNAc(去唾液酸糖蛋白受体ASGPR的配体)(图3),加入的GalNAc部分高亲和性地与ASGPR的结合,随后被内吞进入细胞。ASGPR仅在肝组织中特异性的表达,所以GalNAc偶联修饰可以将小核酸药物靶向到肝组织。
图3.GalNAc偶联修饰[6]
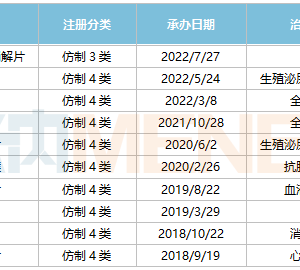
针对 “罕见病” 的核酸类上市药物
目前,针对多种罕见疾病 (如杜氏肌营养不良 (Duchenne muscular dystrophy)、遗传性转甲状腺素蛋白淀粉样变性多发性神经病变 (Transthyretin familial amyloid polyneuropathy)、急性卟啉症 (Acute intermittent porphyria) 等) 的小核酸药物已经获批上市。
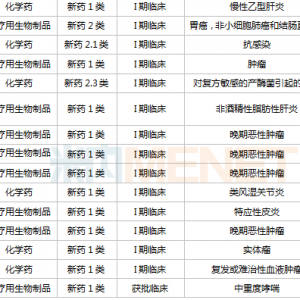
图4. 核酸类上市药物汇总
除上述已上市药物,多款潜在的重要药物也已处于临床开发阶段,覆盖了心血管疾病,肿瘤,乙肝以及多种罕见病领域。
此外,由于具有候选靶点丰富、研发周期短、药效持久、临床开发成功率高等优势,小核酸药物处于生物制药创新的前沿,有望成为继小分子药物、抗体药物之后的第三大类型药物。
参考文献
1. Villalón-García I, Álvarez-Córdoba M, Suárez-Rivero JM, et al. Precision Medicine in Rare Diseases. Diseases. 2020;8(4):42. Published 2020 Nov 13.
2. Faviez C, Chen X, Garcelon N, et al. Diagnosis support systems for rare diseases: a scoping review. Orphanet J Rare Dis. 2020;15(1):94. Published 2020 Apr 16.
3. Rinaldi C, Wood MJA. Antisense oligonucleotides: the next frontier for treatment of neurological disorders. Nat Rev Neurol. 2018;14(1):9-21.
4. Samaridou E, Heyes J, Lutwyche P. Lipid nanoparticles for nucleic acid delivery: Current perspectives. Adv Drug Deliv Rev. 2020;154-155:37-63.
5. Bajan S, Hutvagner G. RNA-Based Therapeutics: From Antisense Oligonucleotides to miRNAs. Cells. 2020;9(1):137. Published 2020 Jan 7.
6. Springer AD, Dowdy SF. GalNAc-siRNA Conjugates: Leading the Way for Delivery of RNAi Therapeutics. Nucleic Acid Ther. 2018;28(3):109-118.
本网页由机器采集生成,若侵权请及时联系删除。
原文链接:https://med.sina.com/article_detail_103_2_114062.html